L’agente eziologico
La neosporosi è provocata da Neospora caninum, un protozoo parassita appartenente al Phylum Apicomplexa, che comprende tutti i protozoi provvisti di complesso apicale, alla Classe Sporozoasida, all’Ordine Eucoccidionida e alla Famiglia Sarcocystidae.
N.caninum ha la proprietà di formare cisti nei tessuti dell’ospite che infetta mediante uno dei 3 principali stadi che si conoscono:
– I tachizoiti di forma allungata (6×2 μm), che rappresentano la forma invasiva del parassita a replicazione rapida e che si moltiplicano nel citoplasma cellulare.
– I bradizoiti contenuti nelle cisti tissutali, ovvero la forma di resistenza parassitaria a replicazione lenta, che si sviluppa nell’ospite intermedio. Le cisti si trovano principalmente a livello del tessuto nervoso, sono di forma allungata o rotondeggiante e hanno una parete spessa (4μm).
– Gli sporozoiti contenuti nelle oocisti, ovvero la forma di resistenza parassitaria nell’ambiente esterno. Le oocisti hanno una forma rotondeggiante, misurano circa 10×12 μm e vengono emesse dall’ospite definitivo. Nell’ambiente esterno diventano infettanti poiché si formano gli sporozoiti dopo circa 24 ore dall’emissione nelle feci (sporulazione).
Ciclo biologico
N.caninum si diffonde nelle popolazioni animali sensibili infettando gli ospiti che possono essere distinti in due categorie, ospiti definitivi e ospiti intermedi a seconda della loro funzione. Gli ospiti definitivi, in cui il parassita svolge la parte intestinale del ciclo, sono il cane (Canis lupus familiaris) e altri canidi selvatici: il lupo (Canis lupus lupus), il dingo (Canis lupus dingo) e il coyote (Canis latrans). Gli ospiti intermedi, in cui il parassita svolge solo la parte extra-intestinale del ciclo, sono numerosi mammiferi domestici e selvatici: il bovino (Bos taurus), la pecora (Ovis aries), la capra (Capra hircus), il cervo (Cervus elaphus), il cavallo (Equus ferus caballus), il bufalo (Bubalus bubalis) e il cane stesso. Il cane si infetta mediante l’ingestione di tessuti e/o organi contenenti cisti tissutali, come feti abortiti e invogli fetali: se in allevamento il cane ha liberamente accesso alle sale parto e alle aree di ricovero degli animali e tali visceri non vengono opportunamente smaltiti, l’infezione è facilitata. Nel cane, l’infezione per via orale determina lo sviluppo del parassita primariamente a livello della mucosa intestinale (tenue) che culmina con la produzione delle oocisti che andranno a contaminare l’ambiente in cui il cane vive o in cui si sposta.
Nel cane è riconosciuta anche una via di trasmissione transplacentare, soprattutto nel caso di cagne infette cronicamente.
I cani sono ospiti completi, infatti, oltre a essere ospiti definitivi nel ciclo di N. caninum emettendo oocisti da 8 a 23 giorni dopo l’infezione, possono anche essere ospiti intermedi, albergando cisti tissutali a livello cerebrale.
Gli ospiti intermedi, tra cui i principali sono i bovini, consentono al parassita di svolgere nel loro organismo solo la parte extra-intestinale del ciclo del parassita e si infettano mediante due principali vie di trasmissione:
– La via orizzontale, attraverso l’ingestione di alimenti o acqua contaminati da oocisti infettanti, ovvero che sono andate incontro a sporulazione dopo l’emissione da parte dell’ospite definitivo, il cane.
– La via verticale, responsabile del mantenimento dell’infezione all’interno degli allevamenti, mediante il passaggio transplacentare dei tachizoiti al feto.
Nella via verticale distinguiamo una trasmissione esogena e una endogena.
La trasmissione esogena avviene quando l’animale gravido contrae l’infezione durante il periodo di gestazione, mediante l’ingestione di oocisti sporulate presenti in ambiente; mentre quella endogena, si ha quando si assiste ad una riattivazione di un’infezione cronica (a sua volta contratta per via orizzontale o congenita) a seguito della replicazione rapida di tachizoiti presenti nelle cisti del tessuto nervoso.
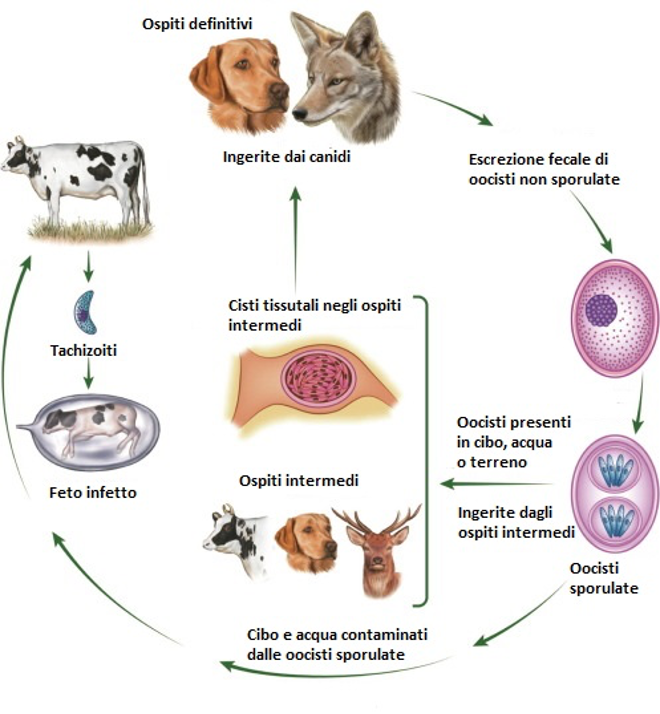
Foto 1: Ciclo biologico di Neospora caninum (tratto da Dubey et al., 2017)
Epidemiologia
La neosporosi è una malattia parassitaria molto diffusa negli allevamenti di bovini da latte che causa importanti ripercussioni sulla efficienza riproduttiva degli animali.
La movimentazione e lo scambio di animali su tutto il territorio europeo, senza l’esecuzione di test sierologici in ingresso e di periodi di quarantena, ha favorito la diffusione di questa patologia anche negli allevamenti italiani.
In Italia, non essendo presenti piani di controllo ufficiali, i dati epidemiologici si deducono dalle analisi effettuate da laboratori, con ampie variabilità dovute ai metodi diagnostici utilizzati, al tipo di allevamento, alla valutazione condotta a livello individuale o aziendale.
Al Nord Italia si stima una sieroprevalenza media di 20% e circa il 50% degli allevamenti registra almeno un capo positivo all’indagine sierologica (Otranto et al., 2003); al Sud la sieroprevalenza è leggermente inferiore, fatta eccezione per la Sardegna, dove nelle aziende di bovini da latte si registrano valori medi di 55% (Varcasia et al., 2006; Otranto et al., 2003). Inoltre, un recente studio condotto in Lombardia su feti abortiti di bovine da latte di razza Frisona ha rilevato, mediante real-time PCR (Polymerase Chain Reaction), una positività molecolare pari al 27,8% (Villa et al., 2021).
Neospora caninum è uno dei principali agenti di aborto infettivo nel bovino e dal punto di vista epidemiologico possiamo distinguere differenti situazioni di circolazione del patogeno in allevamento:
– Una forma abortigena di tipo sporadico con un tasso annuale di aborti inferiore al 3%.
– Una forma endemica: si osserva un tasso di aborti, soprattutto dovuti all’infezione per via transplacentare endogena, costante nel tempo e che può arrivare fino al 10%.
– Una forma epidemica per trasmissione orizzontale: in breve tempo arriva a interessare fino al 30% delle bovine gravide con la comparsa simultanea o in rapida successione di aborti, la cosiddetta “tempesta di aborti”.
Nel caso di N. caninum, le bovine che hanno già abortito possono abortire nuovamente nelle gravidanze successive. Infatti, è stato dimostrato che all’aumentare della sieropositività aumenta il rischio di aborto: le bovine sieropositive presentano un rischio di aborto da 2 a 12 volte superiore rispetto alle bovine sieronegative. Oltre a ciò, si stima che fino al 95% dei vitelli nati da madri positive siano infetti per via congenita, anche senza presentare una evidente sintomatologia clinica.
Impatto economico
La perdita economica dovuta alla neosporosi è causata soprattutto dai problemi riproduttivi a seguito dell’infezione. In particolar modo, il forte impatto economico è legato all’aumento del numero di inseminazioni necessarie per fecondare le vacche, e quindi alla presenza di “repeat breeders” in allevamento, all’allungamento dell’intervallo inter-parto e di quello parto-concepimento e alla perdita della produzione lattea a seguito del fenomeno abortivo.
A livello mondiale si stimano perdite medie che vanno dai 600 milioni a 2 miliardi di dollari all’anno, di cui i due terzi negli allevamenti da latte e un terzo in quelli da carne. Il principale motivo per cui negli allevamenti da latte le perdite sono maggiori è che il costo di un aborto comprende, non solo la perdita del vitello, ma anche la perdita della produzione di una lattazione (Reichel et al.,2013).
Patologia
Neospora caninum è una delle principali e più importanti cause di aborto infettivo nel bovino. Le bovine possono abortire in qualsiasi momento della gestazione, ma la maggior parte degli aborti avviene nell’intervallo temporale compreso fra il terzo e il settimo mese di gravidanza.
Se l’aborto cade nel primo terzo di gravidanza si assiste al riassorbimento dell’embrione e al ritorno in calore della bovina, nel secondo terzo di gravidanza si ha la mummificazione fetale con conseguente aborto oppure la nascita di animali disvitali e sintomatici, mentre nell’ultimo terzo di gravidanza si osserva la nascita di vitelli infetti ma asintomatici. Quest’ultima evenienza rappresenta la principale causa del mantenimento dell’infezione in azienda, in quanto le vitelle nate, che costituiranno la rimonta interna dell’allevamento, non presentano alcun segno clinico fino al momento dell’aborto e del ritorno in calore.
Nei vitelli che nascono infetti e sintomatici i segni clinici rilevabili sono atassia, esoftalmo, debolezza e iperestensione degli arti. Le lesioni istologiche sono caratterizzate da segni di encefalomielite non suppurativa.
Nelle bovine adulte, l’unico segno clinico è l’aborto e il conseguente ritorno in calore.
Negli ospiti definitivi, ovvero i cani, normalmente non si osservano segni clinici. Nel caso di cuccioli infettati per via transplacentare si può assistere ad una grave forma clinica con lo sviluppo di una paralisi ascendente progressiva a partire dagli arti posteriori. Le lesioni istologiche sono caratterizzate da focolai di infiammazione suppurativa e granulomatosa.
Diagnosi nel bovino
Per la diagnosi di neosporosi nel bovino possiamo utilizzare metodi diretti per la ricerca del parassita o indiretti per la ricerca degli anticorpi.
Per procedere correttamente occorre valutare i dati epidemiologici e la storia clinica dell’animale.
Metodi diretti
La diagnosi diretta per la ricerca di Neospora caninum può essere effettuata mediante tecniche immunoistochimiche o mediante tecniche molecolari.
– In passato la principale tecnica diretta utilizzata era l’immunoistochimica (IHC) su tessuti e organi fetali. Questa metodica è molto specifica ma non è in grado di rilevare il parassita se vi è autolisi dei tessuti.
– Ad oggi, la principale metodica diretta utilizzata per la sua alta sensibilità e specificità è la PCR (Polymerase Chain Reaction).
La PCR consente, infatti, di amplificare in poco tempo il DNA partendo da quantità minime di materiale iniziale.
Dopo l’estrazione del DNA, si amplificano regioni target del parassita, tra cui la regione ITS1 e il gene Nc5, attraverso tecniche sia end-point che real-time.
È importante sottolineare che la sola rilevazione del protozoo non sempre rappresenta la prima causa di aborto, infatti la certezza viene raggiunta mediante l’evidenziazione delle caratteristiche lesioni cerebrali e l’associazione della positività molecolare nel feto con quella sierologica nella vacca abortente.
Metodi indiretti
L’esposizione all’infezione si evidenzia per via indiretta ricercando gli anticorpi prodotti dall’animale durante l’infezione, utilizzando differenti metodiche sierologiche.
– La tecnica IFAT (Immunofluorescence antibody test) è stata la prima metodica sierologica utilizzata per diagnosticare la neosporosi nel bovino. I tachizoiti di Neospora caninum fissati su vetrino sono incubati con il siero in esame, si aggiungono gli anticorpi secondari specie-specifici coniugati con un fluorocromo e si leggono i vetrini al microscopio a fluorescenza.
Il principale vantaggio di questo test è che consente di ottenere un titolo anticorpale e proprio per questo, spesso, viene utilizzato come esame di conferma in caso di risultati dubbi ottenuti con altre tecniche.
Il limite maggiore di questa tecnica è che, essendo molto laboriosa, richiede un personale altamente qualificato. Oltre a ciò, i risultati ottenuti sono spesso operatore-dipendenti in quanto sottoposti a una interpretazione soggettiva.

Foto 2: Ingrandimento al microscopio a fluorescenza, in verde si evidenziano i tachizoiti di Neospora caninum
– La tecnica ELISA (Enzyme-linked immunosorbent assay), che include l’antigene o l’anticorpo di fase solida, l’antigene o l’anticorpo marcato con l’enzima e il substrato della reazione enzimatica.
In commercio sono disponibili diversi kit ELISA commerciali, tra cui uno di tipo competitivo. I vantaggi i questa metodica sono il basso costo, la semplicità di esecuzione e la lettura oggettiva dei risultati ottenuti.
Gli svantaggi sono che sono stati segnalati fenomeni di cross-reattività con altri protozoi appartenenti alla famiglia Sarcocystidae, quali Toxoplasma gondii, Besnoitia besnoiti e Sarcocystis spp., e che non si ottiene un titolo anticorpale definito, il che rende necessario l’utilizzo di un altro test diagnostico per quantificare gli anticorpi prodotti dall’animale.
Una ulteriore possibilità diagnostica è offerta dall’Avidity ELISA , che è in grado di differenziare le infezioni acute da quelle croniche.
Oltre all’esame su siero, i test ELISA sono progettati anche per utilizzare come matrice il latte, individuale o di massa.
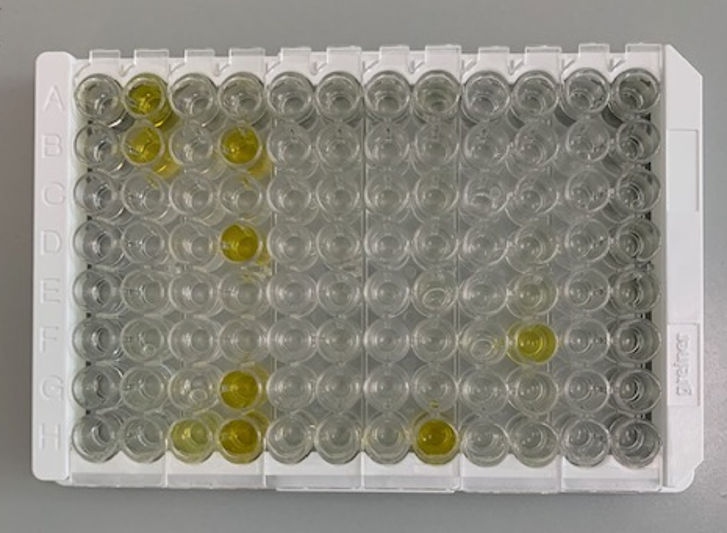
Foto 3: Piastra ELISA, in giallo si evidenziano i pozzetti positivi
In questo caso, i principali svantaggi sono che gli anticorpi nel latte compaiono più tardivamente, sono circa 30 volte meno concentrati e si calcola che all’interno del pool di latte debbano essere presenti almeno 10-15% di animali sieropositivi affinché il campione di latte risulti positivo.
Il latte di massa costituisce comunque un campione facile da prelevare e l’analisi è poco costosa, pertanto un’indagine di questo tipo può essere utile a livello di screening di massa all’interno dell’allevamento.
– Il Western Blot (WB), che è la metodica sierologica più utilizzata come test di conferma dei risultati positivi ottenuti con le precedenti tecniche.
Nel WB gli anticorpi eventualmente presenti nei sieri da esaminare reagiscono con le proteine di N.caninum precedentemente separate mediante elettroforesi su gel di poliacrilamide (SDS-PAGE) e, in seguito, trasferite su una membrana di nitrocellulosa. I limiti maggiori di questa tecnica sono il richiedere molto tempo per l’esecuzione e un personale altamente qualificato.
Considerando che gli anticorpi anti-N. caninum subiscono fluttuazioni durante il periodo di gravidanza, è consigliato testare gli animali nella seconda metà della gestazione, quando i titoli anticorpali raggiungono il picco.
Diagnosi nel cane
Anche nell’ospite definitivo del ciclo parassitario, ovvero il cane, possiamo distinguere metodi diagnostici diretti e indiretti.
– Il principale metodo di diagnosi diretta è l’esame copromicroscopico delle feci per arricchimento (flottazione) con l’utilizzo della soluzione sodio cloruro (NaCl), per verificare l’escrezione delle oocisti di N. caninum .
Un eventuale esito positivo richiede una conferma molecolare in quanto le oocisti sono indistinguibili da quelle di un altro protozoo appartenente alla famiglia Sarcocystidae, ovvero, Hammondia heydorni.
I principali limiti dei metodi diretti sono che solo in pochi casi sono state osservate al microscopio oocisti emesse da feci di animali naturalmente infetti e che la frequenza e durata dell’escrezione delle oocisti, ad oggi, non è nota.
– I principali metodi di diagnosi indiretta nel cane sono la tecnica IFAT e la tecnica ELISA, come nel bovino.
Controllo
Nonostante la grande diffusione della neosporosi negli allevamenti di bovini da latte, questa malattia non è regolamentata né a livello nazionale né europeo: i piani di controllo adottati all’interno dei diversi Stati sono unicamente di tipo volontario. Oltre a ciò, ad oggi, non esistono in commercio né vaccini né trattamenti efficaci per contrastare l’infezione da N. caninum. Sono stati ottenuti buoni risultati con l’utilizzo di toltrazuril nel bovino e di trimethoprim nel cane, ma sono necessari ulteriori studi.
I principali mezzi di controllo sono quelli diretti, che hanno come obiettivo la riduzione della sieroprevalenza aziendale e, quindi, del tasso di aborti annuale.
- Misure di controllo della neosporosi
Se in allevamento sono presenti animali positivi, le strategie che si possono mettere in atto ai fini di contenere la diffusione della malattia sono diverse:
– Test and cull: consiste nel testare tutti gli animali presenti in allevamento mediante sierologia e nell’eliminare tutti i sieropositivi a fine lattazione, sostituendoli con rimonta esterna certificata.
– Fecondazione con seme di toro da carne, preferibilmente di razza Limousine o Piemontese. In queste razze è stata, infatti, dimostrata una maggior resistenza all’infezione e i vitelli nati sono venduti e destinati all’ingrasso, non rimangono in azienda rischiando di diventare i responsabili del mantenimento dell’infezione.
Un recente studio condotto dal nostro gruppo di ricerca in un’azienda da latte in Lombardia ha evidenziato il successo di questo sistema di controllo, applicato sistematicamente per 5 anni: da una situazione di partenza del 33,8%, in termini di sieroprevalenza, e di 15 aborti (3,4%), si è registrata la riduzione sia della sieroprevalenza (28,9% al termine dello studio) che del numero di aborti (5 aborti, 0,9%) al termine del periodo di studio (Sala et al., 2018).
– Embryo-transfer su bovine riceventi sieronegative, nel caso di bovine di alta genealogia.
– Doing nothing: alcuni allevatori adottano questa strategia, ovvero “il non fare nulla” aspettando che N. caninum svolga il suo ciclo all’interno dell’allevamento. Si assiste, quindi, ad una fase iniziale, appena dopo l’entrata del protozoo in azienda, caratterizzata da un elevato numero di aborti; e ad un periodo successivo in cui la mandria sviluppa una copertura anticorpale maggiore e la prevalenza degli aborti si riduce stabilizzandosi sotto il 10%.
- Misure di biosicurezza aziendale
Tali misure sono da adottare all’interno di ogni allevamento ai fini di prevenire l’entrata e la conseguente diffusione della malattia:
– Evitare la contaminazione degli alimenti e dell’acqua di abbeverata con le feci dei cani o degli altri ospiti definitivi.
– Garantire un corretto smaltimento dei feti abortiti e degli annessi fetali.
– Acquistare animali da allevamenti indenni.
– Effettuare periodi di quarantena e test sierologici sugli animali acquistati.
– Vietare l’accesso dei cani negli spazi destinati al ricovero degli animali e degli alimenti e nelle sale parto.
– Istituire un programma di monitoraggio che comprenda l’esame sierologico di tutte le vacche che abortiscono e la ricerca di N. caninum dai feti di vacche sieropositive mediante PCR.
– Controllare le specie infestanti, come i roditori e gli insetti, mediante l’adozione di piani di disinfestazione.
– Regolamentare l’accesso in azienda, per esempio dotando l’azienda di adeguate recinzioni e cancelli che limitino l’ingresso di persone estranee.
– Controllare che venga eseguita una corretta disinfezione del personale e dei mezzi in entrata.



